喜 报
万邦德制药集团有限公司
甲钴胺获美国FDA
授予治疗渐冻症的孤儿药认定
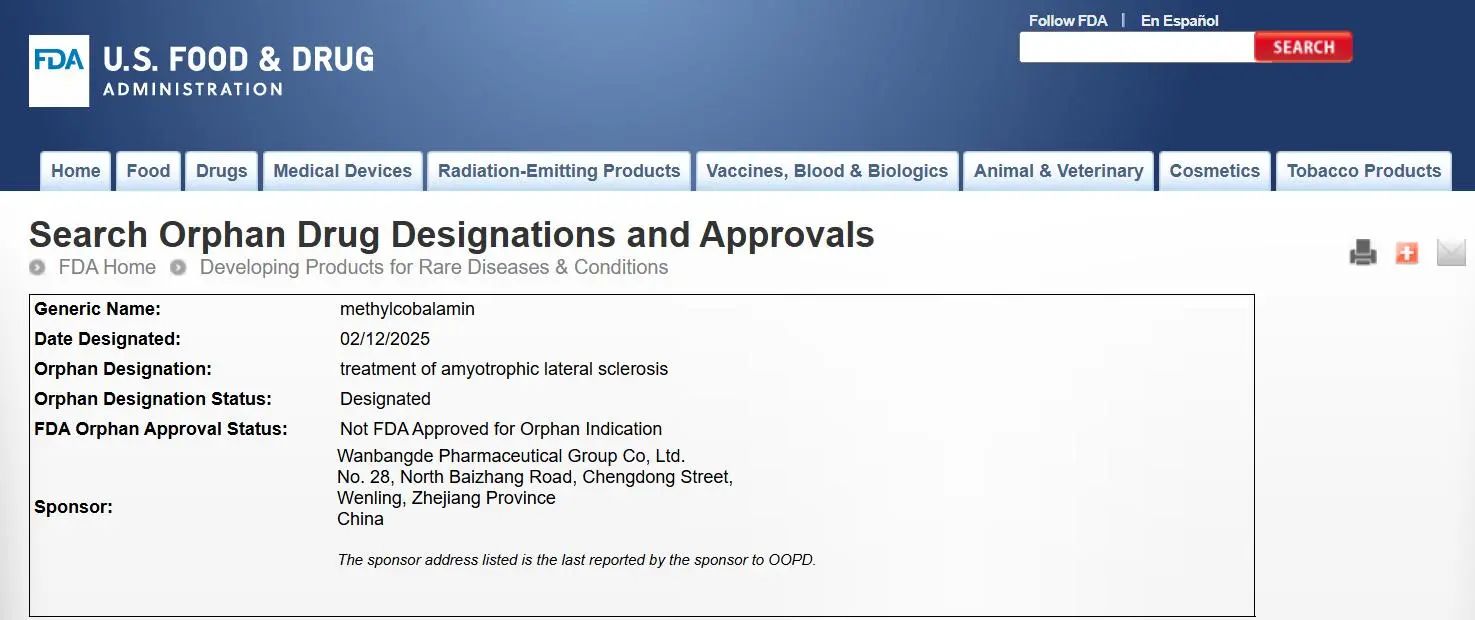
2025年2月14日,万邦德制药集团有限公司宣布,公司的在研新药甲钴胺(methylcobalamin)获得美国食品药品监督管理局(FDA)授予的治疗肌萎缩侧索硬化症(Amyotrophic Lateral Sclerosis, ALS,也称渐冻症)的孤儿药资格认定。
孤儿药(orphan drug)是FDA为鼓励罕见病治疗药物的开发而设立的一种资格认定,为新药开发提供一系列的激励,包括从药品获批开始的7年的市场专营权(market exclusivity)、新药申请(NDA)的优先审评审批、临床开发过程中密切指导与支持,以及新药注册费用的免除。2025年,美国FDA新药注册申请费用为$4,310,002美元(约3100万人民币)。
“我们非常高兴甲钴胺被美国FDA授予治疗渐冻症的孤儿药资格认定,”万邦德制药集团有限公司研发负责人赵冠甲博士表示。“目前我们正在积极推进甲钴胺在全球范围的新药开发,期待全球更多的渐冻症患者能够早日用上这一新的治疗选择。”
关于甲钴胺
甲钴胺是一种维生素B12类似物,也是唯一一种无需生物转化就能穿过血脑屏障的维生素B12。它可以有效地通过体循环运输并储存在肝脏中,但主要被脑细胞,优先是神经元利用。
此次FDA授予的孤儿药资格认定,为公司在渐冻症领域的药品研发,以及公司的国际化布局,提供了有力的支持和保障。
值得一提的是,卫材的甲钴胺冻干粉针于2024年9月在日本获得批准,用于渐冻症的治疗。卫材拥有甲钴胺治疗渐冻症在日本的孤儿药认定,享有在日本市场10年的市场专营权。
关于渐冻症
ALS患者早期症状通常表现为局部肌肉无力或萎缩,如手部握力下降、行走困难或面部僵硬,随后逐渐蔓延至全身,出现肌肉痉挛、言语不清、吞咽困难,甚至因呼吸肌无力而依赖机械通气。部分患者还会伴随情绪波动或认知功能下降,这与大脑额颞叶损伤相关。从确诊起,多数患者生存期仅为2至3年,最终多因呼吸衰竭死亡。
ALS的发病机制复杂,涉及遗传、分子与环境因素的交互作用。约90%的病例为散发性,与遗传无直接关联,而10%的家族性病例中,C9orf72和SOD1基因突变是最常见的遗传诱因。散发性病例虽无明确基因突变,但重金属暴露、吸烟或高强度运动等环境因素可能通过诱发氧化应激和炎症反应加速神经元死亡。全球ALS发病率约为每10万人年1.68例,而美国达到了每10万人4.4例。随着人口老龄化,ALS患病率预计将持续上升。
目前ALS尚无根治手段,治疗以延缓病程、改善生存质量为主。药物利鲁唑通过抑制谷氨酸释放可延长患者生存期约3个月;抗氧化剂依达拉奉能减缓神经功能退化;2023年获批的基因靶向药Tofersen则专门针对SOD1突变患者,阻断毒性蛋白生成。此外,右美沙芬与奎尼丁的组合疗法可缓解情绪失控症状。支持性治疗如无创呼吸机、营养管理和康复训练对改善患者生活至关重要,而干细胞疗法、基因编辑技术等仍处于探索阶段。现有药物普遍存在机制不明、副作用大或费用高昂的局限,多数患者仍面临“无药可医”的困境。
关于万邦德制药集团有限公司
万邦德制药集团始创于1970年,总部位于浙江省台州温岭市,是专业从事现代中药、化学原料药及制剂研发、生产和销售的高新技术企业,注册资本为3.6亿元,现拥有6家子公司,药品生产批准文号185个,涉及14个剂型。公司持续获得“中国医药行业成长50强企业”,“中华民族医药百强品牌企业”,“中国医药工业最具成长力企业”,“中成药企业100强”。公司注册商标被认定为中国驰名商标。
依照“面向患者、面向世界、面向未来”的药品研发理念,公司不仅致力于增强仿制药制剂与原料药的差异化开发的市场竞争力,同时也计划布局1类新药(新化学实体)和依托505(b)(2)路径的2类新药开发。此外,万邦德制药集团还致力于通过布局全球合作加速药品的研发进程,开拓海外市场惠及更广泛的患者群体。这一策略旨在为患者提供更安全、更有效的临床治疗选项,以满足日益增长的临床需求。